Инструкция
1
Радиоактивный углерод с массовым числом 14 постоянно появляется в нижних слоях стратосферы из-за того, что нейтроны космического излучения воздействуют на ядра азота. Свободный углерод встречается в природе в виде графита и алмаза, однако основная его масса приходится на природные карбонаты, горючие газы, каменный уголь, торф, нефть, антрацит и других горючие ископаемые.
2
В земной коре содержится около 0,48% углерода (по массе), в гидросфере и атмосфере он находится в виде диоксида. Примерно 18% углерода на нашей планете входит в состав растений и животных. Его круговорот включает в себя биологический цикл, а также выделение диоксида углерода в атмосферу при сгорании топлива.
3
В биологический цикл входит несколько этапов: сначала углерод из тропосферы поглощается растениями, после чего из биосферы возвращается в геосферу. Вместе с растениями этот химический элемент попадает в организм человека и животных, затем при гниении он переходит в почву, а после этого в виде углекислого газа отправляется в атмосферу.
4
Атомы углерода образуют прочные простые, двойные и тройные связи, что способствует появлению устойчивых циклов и цепей, это является одной из причин существования огромного числа углеродсодержащих органических соединений.
5
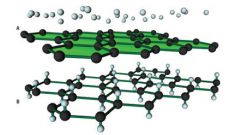
Самые изученные кристаллические модификации углерода — алмаз и графит. Графит термодинамически устойчив в нормальных условиях, алмаз и другие формы являются метастабильными. При температуре выше 1200 К и атмосферном давлении алмаз переходит в графит, причем при 2100 К превращение занимает считанные секунды.
6
При нормальном давлении углерод начинает сублимироваться, когда температура достигает 3780 К, в жидком состоянии он может находиться только при определенном внешнем давлении. Условия прямого перехода графита в алмаз — давление 11-12 ГПа и температура 3000 К.
7
Углерод химически инертен при обычных температурах, но при достаточно высоких он проявляет сильные восстановительные свойства и соединяется со многими элементами. У разных форм углерода отличается химическая активность, она убывает в ряду: аморфный углерод, графит и алмаз. Аморфный углерод и графит вступают в реакцию с водородом при температуре 1200оС, с фтором — при 900оС. Графит взаимодействует с щелочными металлами и галогенами, образуя соединения включения.
Видео по теме