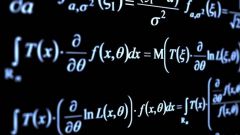Инструкция
1
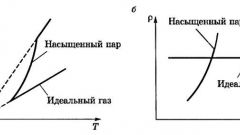
Очень тесную взаимосвязь можно найти между температурой жидкости и атмосферным давлением. Внутри любой жидкости существует много маленьких пузырьков воздуха, имеющих свое внутреннее давление. При нагревании в эти пузырьки испаряется насыщенный пар из окружающей его жидкости. Все это продолжается до тех пор, пока внутреннее давление не станет равным внешнему (атмосферному). Тогда пузырьки не выдерживают и лопаются – происходит процесс, который называется кипением.
2
Аналогичный процесс происходит и в твердых телах при плавлении или при обратном процессе - кристаллизации. Твердое тело состоит из кристаллических решеток, разрушить которые можно при отдалении атомов друг от друга. Давление же, увеличиваясь, действует в обратном направлении – прижимает атомы друг к другу. Соответственно, для того чтобы тело расплавилось, требуется больше энергии и температура повышается.
3
Уравнение Клапейрона-Менделеева описывает зависимость температуры от давления в газе. Формула выглядит так: PV = nRT. Р – давление газа в сосуде. Так как n и R – постоянные величины, становится ясно, что давление прямо пропорционально температуре (при V=const). Это значит, что чем выше Р, тем выше и t. Этот процесс обусловлен тем, что при нагревании межмолекулярное пространство увеличивается, и молекулы начинают двигаться быстро в хаотичном порядке, а значит чаще ударяться об стенки сосуда, в котором находится газ. Температура в уравнении Клапейрона-Менделеева измеряется обычно в градусах Кельвина.
4
Существует понятие стандартной температуры и давления: температура равна -273° по Кельвину (или 0 °С), а давление - 760 мм ртутного столба.
Обратите внимание
Лед имеет высокую удельную теплоемкость, равную 335 кДж/кг. Поэтому, чтобы его растопить, нужно потратить много тепловой энергии. Для сравнения: таким же количеством энергии можно нагреть воду до 80 °С.