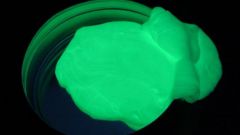
Фосфор - один из биогенных элементов, распространенный как среди животных, так и в неживой природе. У нас фосфор ассоциируется в первую очередь со светящимися брелочками, но это поистине удивительный элемент.

Характеристика фосфора
Судя по положению элемента в таблице Менделеева, сказать можно следующее - расположен в третьем периоде, имеет три электронных уровня, является р-элементом. V группа говорит нам о том, что на внешней орбитали у элемента 5 валентных электронов, отдавая их, он проявляется максимальную степень окисления +5. Это происходит при реакциях с более сильными окислителями, например, кислородом. Оксид проявляет кислотные свойства и при соединении с водой дает фосфорную кислоту. Атом водорода может быть замещен катионами и мы получаем соли - фосфата.
Фосфор может быть и окислителем, например, в соединении с водородом. В этом случае он проявляется валентность III и степень окисления -3, принимая на внешнюю орбиталь три электрона.
Фосфор в природе
Первое, о чем стоит упомянуть, что без этого элемента невозможно было бы существование таких веществ как аденозинтрифосфат - та самая АТФ источник энергии, и фосфолипиды. Фосфор - биогенный элемент. Это значит, что элемент происходит от живых организмов, обязательно присутствует в них.
Как простое вещество фосфор имеет четыре модификации. Белый фосфор крайне ядовит и химически активен. Это летучее вещество с ядовитым запахом, похожим на чеснок. Хранят белый фосфор под слоем воды, в которой он не растворяется. При нагревании белый фосфор переходит в другую модификацию - красный.
Желтый фосфор, по сути, это плохо очищенный белый. также ядовит, имеет неприятный запах. На воздухе загорается зеленым пламенем. В воде не растворим. При сгорании получаются клубы дыма - оксид фосфора.
Красный фосфор - наиболее распространенная модификация. Его можно встретить на спичечных коробках. На воздухе он не загорается, но при трении или детонации активно окисляется (со взрывом - вспомните как чиркает спичка).
Черный фосфор похож на графит по своим физическим характеристикам, является полупроводником. Не растворяется ни в каких растворителях.
Белая и желтая модификации фосфора наиболее активны. Этот элемент образует соединения с металлами, окисляя их, и с неметаллами, выступая в роли восстановителя.
В земной коре содержится 0,09% фосфора. Это довольно высокий показатель. Встретить его можно: в зеленой части растений, плодах и семенах; тканях и костях животных; горных породах, различных минералах; в морской воде.
Биологическая роль фосфора
В нашем организме практически везде можно встретить соединения фосфора. Выше уже была упомянута аденозитрифосфорная кислота - источник энергии. ДНК, РНК, фосфолипиды, фосфопротеиды, различные ферменты - везде есть атомы фосфора.
В различных источниках довольно сухо описывается роль фосфора в организме, но только вдумайтесь - фосфор это обязательная составляющая ДНК - главного информационного носителя нашего организма и АТФ - топлива. Фосфор есть в костях и зубной эмали, если вдруг случается его недостаток - возникают проблемы. А еще вспомните, как нам говорили родители в детстве - ешь рыбу, там фосфор, будешь умным.
Реакции анаболизма и катаболизма, поддержание буферности биологических жидкостей - во всем этом принимают участие соединения фосфора.

Применение соединений фосфора
В чистом виде фосфор применяется очень редко из-за высокой активности и ядовитости. А вот соединения фосфора используются во многих сферах.
Фосфиды - бинарные (состоящие из двух элементов) соединения с металлами используются для получения газа РН3. Он является результатом реакции фосфида с водой или минеральной кислотой (неорганической). Соединения с неметаллами, например, оксид, хлорид, сульфид, галогениды нашли применение в промышленности в качестве осушителей. А на первом месте среди них - оксид пятивалентного фосфора.
Выше уже было упомянуто производство спичек. Высокая реакционная способность фосфора - идеальное свойство для взрывчатых соединений, бомб и определенных видах топлива. Белый фосфор, кстати, используется в производстве дымовых снарядов. Соединения фосфора - это еще и смазочные материалы и защита металлов от коррозии. Некоторые соединения используют для водоочистки, если точнее - для умягчения. Отдельного упоминания заслуживают фосфорсодержащие удобрения.

Фосфор в продуктах
Преимущественно фосфор содержится в продуктах животного происхождения, что, в принципе, понятно. Для человека отличными источниками неорганического фосфора являются: мясо и рыба; молочные и кисломолочные продукты; яйца.
Для человека важны именно неорганические соединения фосфора, которые должны поступать с животной пищей - из растительной они усваиваются намного хуже.
Лидер по содержанию фосфора - сухие дрожжи почти 1300 мг 100 гр продукта. Примерно столько же - в пшеничных отрубях тыквенных семечках. На втором месте находятся молочные продукты и их производные: творог (500 мг на 100 гр), кефир (140 мг), молоко (90 мг). И именно молочные продукты являются идеальным поставщиком фосфора, ведь они содержат еще и кальций.
На третьем месте - рыба и морепродукты.
Решая вопросы об источниках фосфора - выбирайте мясо и молочные продукты. Процент усвоения фосфора из них максимален и достигает 70%, в то время как из растительных - всего 20%.
Выбирая источники фосфора, учитывайте и наличие в продукте кальция. Важно, чтобы фосфора было не меньше. Таким образом, идеальные источники элементов: жирный творог, разнообразные орехи, бобовые, гречка, овсянка, говяжья печень.

Соединения фосфора в пищевой промышленности
Отдельная тема для обсуждения - пищевые добавки. Фосфорсодержащие соединения активно используются в пищевой промышленности. Фосфаты (соли фосфорной кислоты) можно найти в колбасе - они связывают лишнюю влагу и делают колбасу однородной, плотной и сочной, приятной для покупателя. Фосфаты также активно используются в мясной и рыбной консервации, производстве сливочного масла и маргарина, плавленых сырков. По сути, все эти продукты так или иначе присутствуют в нашей продуктовой корзине.
Фосфаты используют в качестве подкислителей в сладких газировках (кстати, именно поэтому говорят что они - газировки - вредны), кондитерских изделиях, слабоалкогольной продукции. В обычную сгущенку фосфаты добавляют, чтобы предотвратить образование кристаллов, а в порошковые добавки, типа сухого молока, какао или сливках - чтобы не было комочков от слеживания. Плавленые сырки имеют однородную структуру тоже благодаря соединениям фосфора.
Осветление сахара, увеличение плотности овощных и фруктовых консервов, сохранность маргарина и масла - все это работа фосфатов. Избыток фосфора приводит к тому, что нарушается усвоение кальция и образование витамина Д. Для организма это значит буквально следующее - кальций изымается из хранилищ - костей и образует с фосфором нерастворимые соединения, которые оседают в виде камней в почках. Это также может вызвать нарушения работы сердечно-сосудистой системы, ЖКТ и печени.
Максимально допустимое соотношения фосфора и кальция 1,5:1. В продуктах соединения фосфора маркируются от Е338 до Е342.