Инструкция
1
Хлорид натрия в чистом виде представляет собой бесцветные кристаллы, но в присутствии примесей может принимать желтый, розовый, фиолетовый, голубой или серый оттенок. В природе NaCl встречается в виде минерала галита, из которого изготавливается бытовая поваренная соль. Огромное количество хлористого натрия растворено также в морской воде.
2
Галит – это прозрачный, бесцветный минерал со стеклянным блеском, имеющий гранецентрированную кубическую решетку (ГЦК-решетку). В нем содержится 60,66% хлора и 39,34% натрия.
3
Температура плавления NaCl – 800,8˚C, кипения - 1465˚C. Он умеренно растворим в воде, причем растворимость слабо зависит от нагревания, но значительно уменьшается в присутствии хлоридов других металлов, гидроксида натрия, хлороводорода. Поваренная соль растворяется в жидком аммиаке и вступает в обменные реакции с другими веществами. Чистый NaCl не гигроскопичен, но в присутствии примесей (Ca(2+), Mg(2+), SO4(2-)) сыреет на воздухе.
4
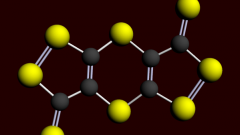
В молекуле NaCl ионная связь между Na и Cl, поскольку натрий и хлор – атомы с большой разностью электроотрицательностей (>1,7). Общая электронная пара в данном случае полностью переходит к атому с большей электроотрицательностью – хлору. В результате образуется положительный ион натрия Na+, отрицательный ион хлора Cl-, и между ними возникает электростатическое притяжение – ионная связь. Ее можно рассматривать как предельный случай ковалентной полярной связи.
5
В процессе образования ионной связи атомы переходят в более устойчивое состояние. Электронные конфигурации ионов завершенные. Но ионная связь отличается от ковалентной, поскольку электростатические силы расходятся от иона во все стороны. Этим обусловлена ненаправленность, а также ненасыщаемость ионной связи.
6
Каждый катион Na+ в кристаллической решетке поваренной соли окружен шестью анионами Cl-, а каждый хлорид-ион окружен, соответственно, шестью ионами натрия. Таким образом, все атомы расположены поочередно в вершинах и центрах граней простой кубической решетки.
Полезный совет
В некоторых веществах, например, щелочах и многих солях, молекулы сочетают в себе ионные и ковалентные связи. Так, связи между атомами натрия и кислорода в молекуле гидроксида натрия NaOH – ионные, а между атомами кислорода и водорода – ковалентные полярные. Аналогичная картина наблюдается для связей Na-S и S-O в молекуле сульфата натрия Na2SO4.