Вам понадобится
- Справочная литература
- База по окислительно-восстановительным потенциалам
- Стандартные электродные потенциалы при 25o С
- Ручка
- Листок бумаги
Инструкция
1
Подобрать химические элементы, которые будут использованы для работы с помощью базы по окислительно-восстановительным потенциалам. Очень часто в таких целях используют сульфат цинка и медный купорос, потому что их очень легко приобрести в любом садоводческом магазине.
2
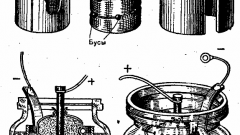
Записать формулу гальванического элемента в стандартном виде. Например:
Zn | ZnSO4 || CuSO4 | Cu
Здесь вертикальная линия обозначает границу раздела фаз, а двойная вертикальная линия – солевой мостик.
Zn | ZnSO4 || CuSO4 | Cu
Здесь вертикальная линия обозначает границу раздела фаз, а двойная вертикальная линия – солевой мостик.
3
Записать электродные полуреакции, пользуясь таблицей электродных потенциалов. Обычно их записывают в виде реакций восстановления. Для нашего примера это выглядит следующим образом:
Правый электрод: +2Cu + 2e = Cu
Левый электрод: +2Zn + 2e = Zn
Правый электрод: +2Cu + 2e = Cu
Левый электрод: +2Zn + 2e = Zn
4
Записать общую реакцию на гальваническом элементе. Она представляет собой разность между реакциями на правом и левом электродах:
+2Cu + Zn = Cu + Zn2+
+2Cu + Zn = Cu + Zn2+
5
Рассчитать потенциалы левого и правого электродов по формуле Нернста.
6
Рассчитать электродвижущую силу (ЭДС) для гальванического элемента. Она, в общем случае, равна разности потенциалов левого и правого электродов. Если ЭДС положительна, то реакция на электродах протекает самопроизвольно. Если ЭДС отрицательна, то самопроизвольно протекает обратная реакция. Для большинства гальванических элементов ЭДС находится в пределах 1.1 Вольта.
Обратите внимание
Старайтесь выбирать те химические элементы, которые не являются токсичными или особо вредными, так как их будет сложно найти в продаже, и они могут нанести непоправимый вред вашему здоровью.
Полезный совет
Перед тем как выбирать вещества для гальванического элемента, посоветуйтесь со специалистом или найдите в справочной литературе, какая пара даст наибольшую положительную разность потенциалов.
Проверьте свои расчеты несколько раз или дайте их на проверку опытному человеку.
Проверьте свои расчеты несколько раз или дайте их на проверку опытному человеку.