Вам понадобится
- - мерная колба
- - пробирка
- - реактивы (HCl, NH₄OH, (NH₄)₂SO₄, NaCl)
Инструкция
1
2
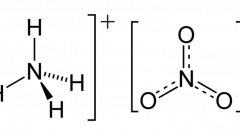
В лаборатории NH₄Cl можно получить при воздействии гидроксида аммония на раствор соляной кислоты. Дополнительные условия не требуются.
Проведение реакции. По химическому уравнению высчитайте, какое количество исходных веществ необходимо взять. Налейте в пробирку высчитанное колличество соляной кислоты (HCl), добавьте раствор гидроксида аммония.
Результат. В результате нейтрализации кислоты гидроксидом образуется соль (хлорид аммония) и вода.
NH₄OH+HCl=NH₄Cl+H₂O
Проведение реакции. По химическому уравнению высчитайте, какое количество исходных веществ необходимо взять. Налейте в пробирку высчитанное колличество соляной кислоты (HCl), добавьте раствор гидроксида аммония.
Результат. В результате нейтрализации кислоты гидроксидом образуется соль (хлорид аммония) и вода.
NH₄OH+HCl=NH₄Cl+H₂O
3
Другой лабораторный метод получения – взаимодействие двух солей.
Проведение реакции. Рассчитайте количество веществ, вступающих в реакцию. Отмерьте раствор хлорида натрия и добавьте раствор сульфата аммония.
Результат. Реакция проходит в два этапа. Сульфат аммония вступает в реакцию с хлоридом натрия. Ион натрия вытесняет ион аммония из его соединения. На промежуточной стадии образуется сульфат натрия, который в дальнейшем в реакции не участвует. На второй стадии аммиак взаимодействует с раствором соляной кислотой. Визуальный эффект реакции – выделение белого дыма.
(NH₄)₂SO₄ +NaCl=Na₂SO₄ + 2HCl+ 2NH₃↑
HCl+NH₃ =NH₄Cl
Для получении хлорида аммония в лаборатории применяют специальный прибор, чтобы получить нужное вещество в твердом виде. Т.к. при повышении температуры хлористый аммоний распадается на аммиак и хлороводород.
Проведение реакции. Рассчитайте количество веществ, вступающих в реакцию. Отмерьте раствор хлорида натрия и добавьте раствор сульфата аммония.
Результат. Реакция проходит в два этапа. Сульфат аммония вступает в реакцию с хлоридом натрия. Ион натрия вытесняет ион аммония из его соединения. На промежуточной стадии образуется сульфат натрия, который в дальнейшем в реакции не участвует. На второй стадии аммиак взаимодействует с раствором соляной кислотой. Визуальный эффект реакции – выделение белого дыма.
(NH₄)₂SO₄ +NaCl=Na₂SO₄ + 2HCl+ 2NH₃↑
HCl+NH₃ =NH₄Cl
Для получении хлорида аммония в лаборатории применяют специальный прибор, чтобы получить нужное вещество в твердом виде. Т.к. при повышении температуры хлористый аммоний распадается на аммиак и хлороводород.
Видео по теме
Обратите внимание
Аммиак и его соли оказывает раздражающее действие на слизистую (он обладает резким запахом). Поэтому при работе с ним необходимо соблюдать технику безопасности:
- не вдыхайте пары аммиака;
- пробирки с реактивами держите от лица на расстоянии.
- не вдыхайте пары аммиака;
- пробирки с реактивами держите от лица на расстоянии.