Вам понадобится
- - градуированный мерный стаканчик;
- - лабораторные весы;
- - стеклянная пипетка;
- - лакмус;
- - раствор щелочи.
Инструкция
1
Предположим, у вас есть емкость с этикеткой H2SO4. То есть сразу становится ясно: в ней содержится серная кислота. Но больше никакой информации нет. Как же определить ее концентрацию? Вы можете сделать это с помощью таблиц плотностей растворов. Существует множество справочников, где приведены значения плотности раствора химических веществ в зависимости от их концентрации.
2
Возьмите градуированный мерный стаканчик, взвесьте его на лабораторных весах. Обозначьте массу пустого стаканчика, как m1. С помощью стеклянной пипетки прилейте в него некоторый объем V серной кислоты. Снова взвесьте стаканчик, обозначьте его массу, как m2. Плотность кислоты находится по формуле: (m2 – m1)/V.
3
По таблице плотностей установите концентрацию раствора. Предположим, в ходе описанного опыта вы вычислили плотность серной кислоты: 1,303 грамм/миллилитр. Ей соответствует 40%-я концентрация.
4
Как еще определяется концентрация кислоты? Есть чувствительный и очень точный метод, который называется прямое титрование. Он основан на реакции нейтрализации кислоты раствором щелочи, концентрация которой известна. Например, в случае с серной кислотой: H2SO4 + 2NaOH = Na2SO4 + 2H2O.
5
По схеме реакции видно, что для нейтрализации одного моля кислоты понадобится два моля гидроксида натрия. Исходя из этого, зная объем исследуемого раствора кислоты, объем щелочи, пошедшей на ее нейтрализацию, а также концентрацию щелочи, можно вычислить и концентрацию кислоты.
6
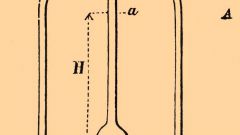
Но как определить точный объем щелочи, необходимой для нейтрализации кислоты? С помощью индикатора, меняющего цвет. Например, лакмуса. Опыт проводится так. Над сосудом с известным объемом кислоты (куда также добавляют несколько капель индикатора) закрепите градуированную бюретку с раствором щелочи.
7
Запишите показание верхнего уровня щелочи, затем, осторожно отвернув кран бюретки, начните по каплям приливать ее к кислоте. Ваша задача – перекрыть кран в тот момент, когда красный цвет индикатора исчезнет. Запишите показание нижнего уровня щелочи и вычислите, какой ее объем ушел на нейтрализацию кислоты.
8
А дальше, зная величину этого объема и точную концентрацию щелочи, легко можно вычислить, сколько молей щелочи вступило в реакцию. Соответственно, количество молей кислоты было в 2 раза меньше. Зная первоначальный объем кислоты, вы найдете ее молярную концентрацию.