Вам понадобится
- - периодическая таблица химических элементов;
- - герметичный баллон;
- - весы;
- - манометр;
- - термометр.
Инструкция
1
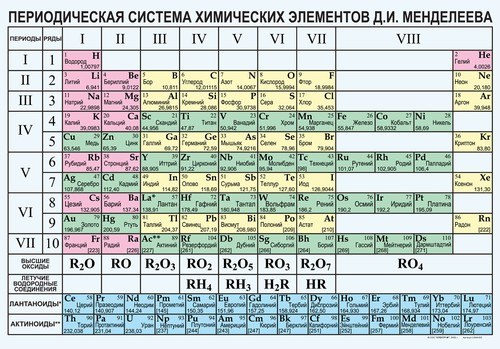
Если известна химическая формула вещества определите его молекулярную массу, используя периодическую таблицу химических элементов Менделеева. Для этого определите элементы, которые входят в формулу вещества. Затем, найдите их относительные атомные массы, которые записаны в таблице. Если атомная масса в таблице представлена дробным числом, округлите ее до ближайшего целого. Если химическая формула содержит несколько атомов данного элемента, умножьте массу одного атома на их количество. Полученные атомные массы сложите и получите относительную молекулярную массу вещества.
2
Например, чтобы найти молекулярную массу серной кислоты H2SO4, найдите относительные атомные массы элементов, которые входят в формулу, соответственно водорода, серы и кислорода Ar(H)=1, Ar(S)=32, Ar(O)=16. Учитывая, что водорода в молекуле 2 атома, а кислорода 4 атома, рассчитайте молекулярную массу вещества Mr(H2SO4)=2•1+32+4∙16=98 атомных единиц массы.
3
В том случае, если известно количество вещества в молях ν и масса вещества m, выраженная в граммах, определите его молярную массу для этого массу поделите на количество вещества M=m/ν. Она будет численно равна его относительной молекулярной массе.
4
Если известно количество молекул вещества N, известной массы m, найдите его молярную массу. Она будет равна молекулярной массе, найдя отношение массы в граммах к количеству молекул вещества в этой массе, а результат умножьте на постоянную Авогадро NА=6,022^23 1/моль (M=m∙N/ NА).
5
Чтобы найти молекулярную массу неизвестного газа, найдите его массу в герметичном баллоне известного объема. Для этого откачайте газ из него, создав там вакуум. Взвесьте баллон. Затем закачайте газ обратно и снова найдите его массу. Разность масс пустого и закачанного баллона и будет равна массе газа. Измерьте давление внутри баллона при помощи манометра в Паскалях, а температуру в Кельвинах. Для этого измерьте температуру окружающего воздуха, она будет равна температуре внутри баллона в градусах Цельсия, чтобы перевести ее в Кельвины, прибавьте к полученному значению 273.
Определите молярную массу газа, найдя произведение температуры T, массы газа m и универсальной газовой постоянной R (8,31). Полученное число поделите на значения давления P и объема V, измеренного в м³ (M=m•8,31•T/(P•V)). Это число будет соответствовать молекулярной массе исследуемого газа.
Определите молярную массу газа, найдя произведение температуры T, массы газа m и универсальной газовой постоянной R (8,31). Полученное число поделите на значения давления P и объема V, измеренного в м³ (M=m•8,31•T/(P•V)). Это число будет соответствовать молекулярной массе исследуемого газа.