Инструкция
1
В Старом Свете платина стала известна после XVI века, но коренные американцы добывали ее очень много столетий до этого. Так, в 1557 году европеец Скалинтер в своей книге «Экзотические упражнения в 15 книгах» рассказал о металле, который добывают в Гондурасе и который очень трудно плавится. Но после открытия конкистадорами Нового Света платина не сразу стала популярной в Европе, так как долго время считалась металлом вредным. Подобную репутацию этому химическому элементу обеспечило свойство легкого сплавления с золотом, чем и пользовались фальшивомонетчики. Тогда король Испании даже запретил ввозить платину в страну, а уже имеющийся в Испании металл вывести за пределы городов и утопить в море. Алхимики стали производить эксперименты с металлом только в 1820 году.
2
В настоящее время уже известно, что самые массовые месторождения платины находятся в ЮАР, Китае, США, Зимбабве и в России. Платиновые самородки обычно добывают на приисках способом так называемого шлихового опробывания. Так металлический концентрат растворяют в царской водке, затем добавляют в нее этанол и сахарный сироп, которые удаляют избыток вещества HNO3, дальше к ним прибавляют хлорид аммония, после чего получается высушенный остаток, прокаливаемый при 800-1000оС.
3
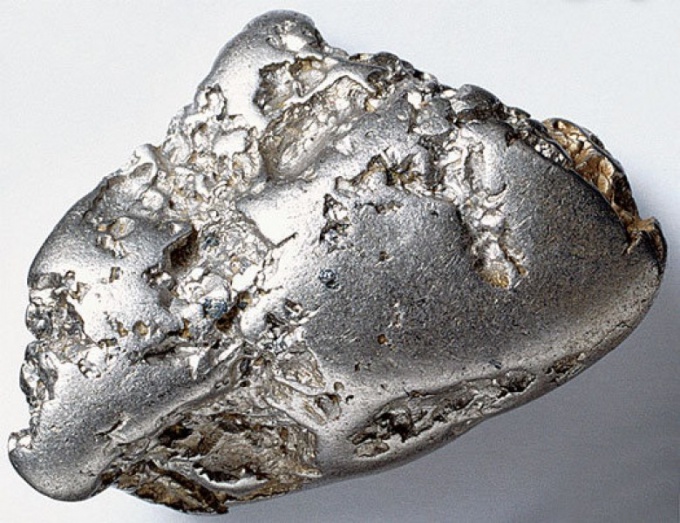
Цвет платины – серебристо или серовато-белый. К физическим свойствам этого химического элемента также относятся следующие: температура плавления при 1768,3оС, в кипения – 3825оС. Платина также является рекордсменом среди других металлов по своей тяжести и плотности, ее очень мало в земной коре.
4
Ученые считают, что по химическим свойствам платина схожа с палладием, но все же проявляет немного большую химическую активность. Причем она вступает в реакцию лишь с горячей царской водкой. Известно, что металл может растворяться (очень медленно) только в концентрате серной кислоты и в жидком броме, другие кислоты (и минеральные, и органические) не оказывают на платину такого же воздействия. В случае нагревания платина способна реагировать с другими элементами – серой, селеном, теллуром, кремнием и углеродом. Она может растворять молекулярный водород и образовывать после взаимодействия с кислородом летучий осадок.
5
Самое частое применение платины – в качестве катализатора при сплаве с родием. Она также очень востребована в ювелирной отрасли, медицине и стоматологии. В производстве лазерной техники из нее делают специальные зеркала и электромагнитные реле.
Видео по теме