Инструкция
1
Один моль того или иного вещества представляет собой такое его количество, которое содержит столько структурных единиц, сколько атомов содержится в 0,012 кг обычного (не радиоактивного) изотопа углерода. К структурным единицам вещества относятся молекулы, атомы, ионы и электроны. Когда в условиях задачи дано вещество с относительной атомной массой Ar, из формулы вещества, в зависимости от постановки задачи, путем осуществления вычислений находят либо массу одного моля этого же вещества, либо его молярную массу. Относительной атомной массой Ar называют величину, равной отношению средней массы изотопа элемента к 1/12 массы углерода.
2
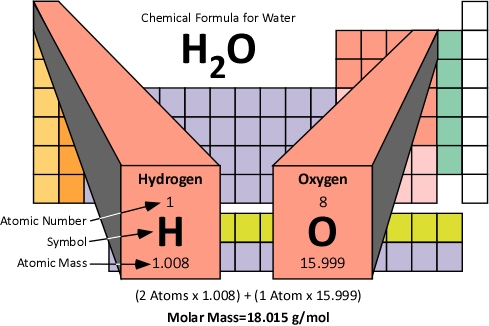
Молярную массу имеют как органические, так и неорганические вещества. Для примера рассчитайте этот параметр в отношении воды H2O и метана CH3. Вначале найдите молярную массу воды:
M(H2O)=2Ar(H)+Ar(O)=2*1+16=18 г/моль
Метан представляет собой газ органического происхождения. Это означает, что в состав его молекулы входят атомы водорода и углерода. Всего в одной молекуле этого газа содержится три атома водорода и один атом углерода. Молярную массу данного вещества рассчитайте следующим образом:
M(CH3)=Ar(C)+2Ar(H)=12+3*1=15 г/моль
Аналогичным образом рассчитывайте молярные массы любых других веществ.
M(H2O)=2Ar(H)+Ar(O)=2*1+16=18 г/моль
Метан представляет собой газ органического происхождения. Это означает, что в состав его молекулы входят атомы водорода и углерода. Всего в одной молекуле этого газа содержится три атома водорода и один атом углерода. Молярную массу данного вещества рассчитайте следующим образом:
M(CH3)=Ar(C)+2Ar(H)=12+3*1=15 г/моль
Аналогичным образом рассчитывайте молярные массы любых других веществ.
3
Также массу одного моля вещества или молярную массу находят, зная массу и количество вещества. В этом случае молярная масса рассчитывается как отношение массы вещества к его количеству. Формула при этом выглядит следующим образом:
M=m/ν, где M - молярная масса, m - масса, ν - количество вещества.
Молярная масса вещества выражается в граммах либо килограммах на моль. Если известна масса молекулы того или иного вещества, то, зная число Авогадро, можно найти массу одного моля вещества следующим образом:
Mr=Na*ma, где Mr - молярная масса, Na - число Авогадро, ma - масса молекулы.
Так, например, зная массу атома углерода, можно найти молярную массу этого вещества:
Mr=Na*ma=6,02*10^23*1,993*10^-26=12 г/моль
M=m/ν, где M - молярная масса, m - масса, ν - количество вещества.
Молярная масса вещества выражается в граммах либо килограммах на моль. Если известна масса молекулы того или иного вещества, то, зная число Авогадро, можно найти массу одного моля вещества следующим образом:
Mr=Na*ma, где Mr - молярная масса, Na - число Авогадро, ma - масса молекулы.
Так, например, зная массу атома углерода, можно найти молярную массу этого вещества:
Mr=Na*ma=6,02*10^23*1,993*10^-26=12 г/моль
Видео по теме